| 放射科设备 |
| 超声科设备 |
| 手术室设备 |
| 检验科设备 |
| 实验室设备 |
| 理疗科设备 |
| 急救室设备 |
| 儿科设备 |
| 眼科设备 |
| 牙科设备 |
| 妇科男科设备 |
| 灭菌消毒设备 |
| 医用教学模型 |
| 美容仪器设备 |
| 家庭保健器具 |
| CR病床 推车 柜 |
| ABS病床轮椅 |
| 医用耗材 |
新闻中心
上海个例医疗器械不良事件报告指南(2023年修订版)发布
刚刚,上海市药品监督管理局发布《上海市个例医疗器械不良事件报告指南(2023年修订版)》,内容如下:
上海市个例医疗器械不良事件报告指南
(2023年修订版)
1. 前言
依据《医疗器械监督管理条例》(中华人民共和国国务院令 第739号)(以下简称《条例》)和《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局 中华人民共和国国家卫生健康委员会令 第1号)(以下简称《办法》),制定本指南。本指南所称医疗器械注册人及备案人(以下简称注册人)与《办法》中所称医疗器械上市许可持有人内涵相同。
本指南旨在指导医疗器械注册人、生产经营企业和使用单位(医疗机构)针对已上市医疗器械收集、识别、填写、报告个例医疗器械不良事件用。
本指南并无法规上的强制执行义务,仅代表编写机构对已上市医疗器械报告个例医疗器械不良事件的想法及建议。本指南是在现行法规及当前技术认知水平下制定的,随着法规的不断完善和科学技术的不断发展,本指南相关内容也将适时进行调整。
特别说明:《办法》明确,医疗器械不良事件报告的内容、风险分析评价报告和统计资料等是加强医疗器械监督管理、指导合理用械的依据,不作为医疗纠纷、医疗诉讼和处理医疗器械质量事故的依据。对于属于医疗事故或者医疗器械质量问题的,应当按照相关法规的要求另行处理。
2. 范围
本指南适用于医疗器械注册人、生产经营企业和使用单位针对在中国已上市医疗器械个例医疗器械不良事件收集、识别、填写、报告用。本指南不包括发生在境外的个例医疗器械不良事件的报告要求,也不包括群体性医疗器械不良事件中个例报告的要求。
注:生产企业指:医疗器械注册人制度下,不持有医疗器械注册证书的医疗器械受托生产企业。
3. 术语和定义
3.1注册人[1]:医疗器械注册人、备案人,是指取得医疗器械注册证或者办理医疗器械备案的企业或者研制机构。
3.2医疗器械使用单位[1]:是指使用医疗器械为他人提供医疗等技术服务的机构,包括医疗机构、计划生育技术服务机构、血站、单采血浆站、康复辅助器具适配机构等。
3.3医疗器械不良事件[2]:是指已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。
3.4严重伤害[2]:是指有下列情况之一者 :
1) 危及生命:在此是指在发生不良事件时患者已经处于死亡的危险中,并不是指假设该不良事件如果更严重可能导致死亡[3]。
2) 导致机体功能的永久性伤害或者机体结构的永久性损伤;
3) 必须采取医疗措施干预才能避免上述永久性伤害或者损伤。
3.5可能导致死亡或严重伤害的医疗器械不良事件[4]:是指没有发生死亡或严重伤害,但如果该事件再次发生,可能导致患者、使用者或其他人的死亡或严重伤害。
3.6非正常使用(异常使用)[4]:是指医疗器械的操作者或使用者的行为导致的结果超出制造厂商任何合理的风险控制方法所能覆盖的范围。
注:在用尽所有其他合理的风险控制手段的情况下,使用说明书中警告的可预见的误用被视为异常使用。
3.7投诉[6]:宣称已从组织的控制中放行的医疗器械存在与标识、质量、耐用性、可靠性、可用性、安全或性能有关的缺陷或宣称影响这些医疗器械性能的服务存在不足的书面、电子或口头的沟通。
3.8使用错误[7]:使用医疗器械时导致不同于制造商预期或用户期望结果的用户动作或用户动作缺失。
注1:使用错误包括用户无能力完成某项任务。
注2:使用错误可能由用户、用户接口、任务或使用环境的特性之间的不匹配造成。
注3:用户可能意识到或未意识到使用错误已经发生。
注4:患者非预期的生理反应本身不视为使用错误。
注5:导致非预期结果的医疗器械故障不视为使用错误。
3.9故障[8]:器械未能满足其性能规范,或者未能按预期发挥作用。性能规范包括器械标签中的所有声明。器械的预期性能是指器械标签中说明的预期用途或者器械上市销售的预期用途。
4. 医疗器械不良事件上报原则
医疗器械不良事件上报遵循以下两个基本原则:
4.1 依法原则
医疗器械注册人、生产经营企业和使用单位应当遵循《条例》和《办法》等相关法规规章规定的原则、职责、程序和时限等要求进行医疗器械不良事件的报告,报告内容应当真实、完整、准确。
(1)导致或者可能导致严重伤害或者死亡的可疑医疗器械不良事件应当报告。
(2)创新医疗器械在首个注册周期内,应当报告该产品的所有医疗器械不良事件。
(3)报告医疗器械不良事件应当遵循可疑即报的原则,即怀疑某事件为医疗器械不良事件时,均可以作为医疗器械不良事件进行报告。
4.2 风险管理原则
注册人应当将风险管理 贯穿于产品设计开发、生产、销售和售后服务等医疗器械全生命周期的过程中,制定风险管理的要求并形成医疗器械特定的风险管理文档。
注册人的风险管理过程要包含医疗器械上市后的风险管理活动,即积极主动收集医疗器械上市后的信息,包括来自使用者、安装保养者的信息,社会公布的信息,以及先进技术的总体认知等信息,并对其中可能和安全相关的信息进行评价,特别是下列方面:
(1) 是否出现先前没有认识的风险(源)或危险情况;
(2) 是否由一个危险情况产生的一个估计的风险不再是可接受的;
(3) 是否与医疗器械预期用途利益相关的剩余风险不再是可接受的;
(4) 是否先进技术的总体认知已经改变。
如果上市后的信息经过评价和安全相关时,注册人要对该医疗器械采取以下行动:
-审评医疗器械的风险管理文档是否需要对风险进行再评定或者对新的风险进行评定;
-当剩余风险不再是可接受时,对先前实施的风险管理活动的影响予以评价,作为一项输入反馈到风险管理过程中;
-考虑对已在市场上的医疗器械的行动需要。
注册人结合医疗器械风险管理文档,对于医疗器械上市后信息中导致死亡或伤害的严重度符合法规报告要求的事件,或者对于医疗器械上市后信息风险分析评价结果为风险不可接受的,应当作为医疗器械不良事件进行报告。对于风险严重度的判断,适宜时要征询医疗机构(临床医护人员)意见。
根据以上两项基本原则,我们将临床发生的事件分为以下三种:
(1) 应当报告的医疗器械不良事件(参见6);
(2) 可以报告的医疗器械不良事件(参见7);
(3) 不需要报告的事件 (参见8)。
注意:为避免因收集途径不同而导致的重复报告,注册人应对收集到的不良事件进行查重,剔除重复信息后上报。如果不能确定是否重复则应当报告。经营企业和使用单位获知注册人已经报告的不良事件,无需进行重复上报。
5. 医疗器械不良事件报告程序和报告时限
已上市的医疗器械发生不良事件时,注册人、生产经营企业和使用单位应当依照法定报告程序和报告时限,参考本指南上报医疗器械不良事件报告。
5.1报告程序
注册人、生产经营企业和使用单位对发生的医疗器械不良事件应及时开展收集、识别、填写和报告。
注册人应当建立医疗器械不良事件监测体系,主动收集来自医疗器械生产经营企业、使用单位、使用者等的不良事件信息,按要求及时向监测机构如实报告医疗器械不良事件。
医疗器械使用单位、生产经营企业应主动维护其用户信息,收集医疗器械不良事件信息,及时向注册人报告,在无法明确注册人或该事件为疑似医疗器械相关的死亡事件的情况下,需要向监测机构报告。生产经营企业和使用单位应确保报告的真实性、完整性和准确性,如果后续取得了初次报告提交时尚未能取得的信息,及时告知注册人,由注册人将此类信息补充完整。
注册人、生产经营企业和使用单位应当在“国家医疗器械不良事件监测信息系统” (以下简称监测信息系统)注册成为用户,网址:https://maers.adrs.org.cn,通过该系统报告医疗器械不良事件。
5.2报告时限
注册人、生产经营企业和使用单位发现或者获知可疑医疗器械不良事件后,导致死亡的应当在7日 内报告;导致严重伤害、可能导致严重伤害或者死亡的应当在20日内报告。
创新医疗器械除了上述情况外的不良事件应当在20日内报告。
注册人在报告医疗器械不良事件后或者通过国家医疗器械不良事件监测信息系统获知相关医疗器械不良事件后,应当按要求开展后续调查、分析和评价,导致死亡的事件应当在30日内,导致严重伤害、可能导致严重伤害或者死亡的事件应当在45日内向注册人所在地省级监测机构报告评价结果。对于事件情况和评价结果有新的发现或者认知的,应当补充报告。
6. 应当报告的医疗器械不良事件
应当报告的不良事件是指4.1(1)(2)所指的不良事件。
4.1(1)即严重伤害或者死亡事件合理的表明是由于医疗器械的原因导致,或者当前没有发生严重伤害和死亡,但医疗器械再次出现类似的情形,可能导致严重伤害 或者死亡。
4.1(2)即在首个注册周期内的创新医疗器械导致或可能导致人体伤害的各种有害事件,伤害的程度不仅限于严重伤害和死亡。
注册人结合医疗器械风险管理文档,对于医疗器械上市后信息中导致死亡或伤害的严重度符合法规报告要求的事件,或者对于医疗器械上市后信息风险分析评价结果为风险不可接受的,应当作为医疗器械不良事件进行报告。对于风险严重度的判断,适宜时要征询医疗机构(临床医护人员)意见。
注册人、生产经营企业、使用单位发现或者获知应当报告的医疗器械不良事件时,应当及时通过监测信息系统报告。生产经营企业、使用单位还应及时告知注册人。
6.1 导致死亡或严重伤害的事件
实际上发生了死亡或严重伤害的事件,且合理的表明是由于医疗器械的原因导致。
案例分享:
有源医疗器械案例:
例1:患者因尿毒症长期在医院血液透析中心行透析治疗。某日护理人员发现患者在透析时突然出现烦躁不安,立即查看病人情况,发现透析管路静脉端脱落,出血量大约300ml,但机器并未出现报警提示立即快速回血,报告值班医生,终止透析,并予0.9%氧化钠注射液快速静脉滴入,持续心电监护,吸氧等抢救治疗。抢救无效,患者于当日死亡。
例2:在使用C型臂X射线系统对患者进行检查的过程中,C型臂的动作失去了控制,患者被击中并致肩部骨折,立即采取了治疗。
无源医疗器械案例:
例1:肿瘤患者进行化疗时,输液港导管破裂发生药液外渗,导致患者外渗处皮肤肿胀、潮红,立即拔出器械并对患者外渗处皮肤给予药物外敷治疗。
体外诊断医疗器械案例:
例1:检验科操作人员正常装载试剂时由于试剂瓶漏液,造成其接触液体引发了过敏性休克。
6.2 可能导致死亡或严重伤害的事件
是指没有发生死亡或严重伤害,但如果该事件再次发生,可能导致患者、使用者或其他人的死亡或严重伤害。
如,医疗器械临床使用过程中发生故障虽然没有导致死亡或严重伤害,但是如果故障再次发生,可能导致死亡或严重伤害。
案例分享:
有源医疗器械案例:
例1:患者因“冠心病”到院治疗,拟使用移动式C型臂X光机进行“冠状动脉介入治疗术”,当日患者进入导管室进行术前穿刺,穿刺成功后使用移动式C型臂X光机进行冠脉造影检查,此时设备出现Err16407/80报警提示,显示屏变成雪花状,且无图像显示,立即联系厂商工程师,按工程师要求重启设备,设备重启后仍然报警,显示屏无图像显示,立即中断手术检查,将患者送往其它医院继续手术,期间患者未诉特殊不适。此次事件考虑设备球管损坏,导致手术被迫中断,造成患者二次手术,但未对患者造成严重伤害。
无源医疗器械案例:
例1:患者行气管插管术后,气囊破裂漏气,医护人员及时发现,立即更换气管插管,患者情况一切正常。如果再次发生,医护人员没有及时发现,可能导致患者受到严重伤害甚至危及患者生命。
体外诊断医疗器械案例:
例1:一名患者梅毒在化学发光仪上检测结果阴性,用户将该结果报告至临床,医生质疑结果与临床不符,用户使用另一厂家仪器检测结果为阳性。类似假阴性结果如果再次发生,可能会造成医生对疾病的漏诊,导致患者未能及时接受治疗,可能造成疾病的传播。
6.3 创新医疗器械的不良事件
有源医疗器械案例:
例1:患者为治疗房颤,使用某创新医疗器械消融导管,导管就位后无法放电,指示灯一直闪烁,更换连接尾线,故障也无法排除,后续更换同品牌同型号导管后手术顺利完成。
无源医疗器械案例:
例1:经导管瓣膜置换手术过程中,护士发现装有生物瓣膜的容器外外表面有水渍,怀疑容器有裂缝或盖不紧,担心无菌性遭到破坏,随即停止使用该产品,并启用备用产品。
7. 可以报告的医疗器械不良事件
医疗器械不良事件报告需要遵循可疑即报的原则,即怀疑某事件为医疗器械不良事件时,均可以作为医疗器械不良事件进行报告。需要注意的是,注册人、生产经营企业及使用单位需要多方配合尽最大努力收集/提供不良事件相关信息,来判断医疗器械不良事件并决定是否报告,如果经过风险分析评价确定可疑不良事件符合法规报告要求的,应当作为医疗器械不良事件进行报告。
可以报告的医疗器械不良事件涉及以下:
7.1 可疑医疗器械不良事件
7.1.1无法排除伤害是医疗器械导致
医疗器械注册人、生产经营企业、使用单位无法排除伤害是医疗器械导致或者无法获知伤害发生时医疗器械是否发生了故障。
案例分享:
无源医疗器械案例:
例1:患者患有肾功能衰竭,在植入腹主动脉覆膜支架期间虽因多器官功能衰竭而死亡,由于无法对支架的情况进行检测,因此无法排除是支架导致患者死亡。遵循可疑即报原则进行报告。
例2:患者患有冠心病及多支病变,身体条件较为虚弱,护士正常为患者抽血时,采用一根紫色4ML和绿色4ML的采血管,采血过程中,采血管产生可疑正压并将气泡推入病人血管中,致使患者发生鼓包现象,护士长闻讯过来重新采血,并发生同样状况,此后将注射器针头插入采血管中,注射器按钮被从2ML推至5ML,患者抽血前无异样状况发生。5日后患者由于心力衰竭去世,无法判断采血管空气进入对患者病情发展的影响,遵循可疑即报原则进行报告。
有源医疗器械案例:
例1:医院在使用离心泵治疗过程中发现设备不能显示流量,此时患者生命垂危。医护人员用手摇柄维持离心泵工作,继续为患者治疗,后患者死亡,无法获知离心泵故障是否导致患者死亡,遵循可疑即报原则进行报告。
7.1.2无法排除伤害是医疗器械操作导致
医疗器械注册人、生产经营企业、使用单位无法排除伤害是医疗器械操作导致。
案例分享:
无源医疗器械案例:
例1:患者为72岁男性,既往史不详,因心梗接受心脏介入手术植入支架。造影显示LAD中段狭窄率为90-100%,一般迂曲,无钙化,无血栓。术中成功植入第一枚支架再次植入另一枚支架过程中血管破裂,施救无效,宣布死亡。无法确定术中是否存在操作问题导致血管破裂,遵循可疑即报原则进行报告。
有源医疗器械案例:
例1:女性患者年纪较大,具体年龄不详,视力不好,因糖尿病使用胰岛素注射泵,后突发死亡,死亡时具体血糖数值不详。不排除患者超剂量使用胰岛素,导致低血糖的可能。遵循可疑即报原则进行报告。
7.1.3无法判断死亡、伤害与患者自身疾病的关联性
医疗器械注册人、生产经营企业、使用单位无法识别死亡、伤害是否与患者原患疾病有关。
案例分享:
无源医疗器械案例:
例1:患者为67岁男性,既往史不详,因心肌梗塞接受心脏介入手术植入支架。造影显示LCX近段狭窄率为100%一般迂曲,无钙化,轻度血栓。经球囊以10atm预扩后,植入支架后发现LCX内血流变慢,考虑支架内血栓形成,对症处理后血流恢复,手术结束。但患者术后1小时突然出现心源性脑缺血综合症,抢救无效于手术当天死亡。术者认为可能与患者原患疾病有关,遵循可疑即报原则进行报告。
例2:患者为71岁女性,有慢性肾衰、心衰、高血压史40年,因腹透感染转血透治疗后内瘘闭塞经右颈内静脉植入血液透析管。2个月后患者在做透析时发现导管隧道出口附近有漏血。据患者家属反馈透析前护士消毒时曾用镊子夹持导管。由于当时患者未有其他不适,经临床评估无须立即做换管操作。3日后患者进行换管手术,术中无超声引导,术前未使用X光检查,在拔出原导管后,术者与患者家属交流过程中患者突发心脏骤停,抢救无效死亡。怀疑患者死亡为自身疾病导致,遵循可疑即报原则进行报告。
7.2导致或者可能导致一般伤害(非严重伤害和死亡)的医疗器械不良事件
7.2.1导致一般伤害(非严重伤害和死亡)的医疗器械不良事件
案例分享:
有源医疗器械案例:
例1:患者为69岁男性,需进行心电监护,使用一次性使用心电电极18小时后,患者描述电极粘贴处皮肤瘙痒,护士取下电极后发现粘贴部位发红,立即停用心电电极,对症处理,一天后症状缓解。
无源医疗器械案例:
例1:护士为患者进行留置针,操作成功后发现留置针管路接头处有漏血,拔针后更换新的留置针,再次穿刺,操作成功,未对患者造成严重伤害。
例2:一次性使用采血针针帽缺失,检验师在取用时不小心触碰裸露的针尖,感到刺痛,随即检查发现手套被刺破,但皮肤并未破损,更换其他批次产品。
7.2.2可能导致一般伤害(非严重伤害和死亡)的医疗器械不良事件
1.医护人员临床使用前发现的质量问题
案例分享:
无源医疗器械案例:
例1:医护人员临床使用前检查发现,一次性使用的介入耗材存在被污染的痕迹或部件缺损等质量问题,可能会导致感染或异物残留患者体腔。遵循可疑即报原则进行报告。
体外诊断医疗器械案例:
例1:医护人员临床使用前检查发现,试剂盒质量问题导致试剂漏液,可能会导致检测过程中吸样不足,造成检测结果错误。遵循可疑即报原则进行报告。
2.医疗器械网络安全事件
案例分享:
例1:由于医疗器械潜在缺陷,引起网络安全问题,可能导致未经授权的医疗器械远程访问,患者隐私或器械功能可能受到侵犯,遵循可疑即报原则进行报告。
3.医疗器械合并使用的相互作用
案例分享:
有源医疗器械案例:
内窥镜和润滑剂联合使用时,由于润滑剂与患者体腔内液体产生化学反应,导致起雾医生无法看清腔体内影响,内窥镜可能会刮伤患者粘膜。
体外诊断医疗器械案例:
在使用高敏肌钙蛋白T检测试剂盒时,使用部分制造商的K2/K3 EDTA采血管进行采样和样本处理时,可能导致样本污染,导致高敏肌钙蛋白T检测结果错误升高。
4.使用错误可能导致的一般伤害
案例分享:
护士误用石蜡油润滑乳胶导尿管,可能导致导尿管球囊破裂,患者需要更换导尿管。
8. 不需要报告的事件
以下不符合医疗器械不良事件定义,不需要按照医疗器械不良事件报告的事件,并不免除其按照其他法规报告的义务,如:医疗器械临床试验过程中发生的不良事件要按照医疗器械临床试验相关规定报告,使用前发现医疗器械故障或缺陷可以按照产品质量投诉程序向注册人或经营企业反馈。注册人需要对投诉进行收集、分析、处理。
在上报时限内无法确认以上情况时,应遵循可疑即报的原则,按照医疗器械不良事件报告。
8.1使用未获得注册证/备案凭证医疗器械导致的伤害或死亡事件
医疗器械上市前 临床试验过程中出现的导致人体伤害或死亡的各种有害事件。
8.2非正常使用医疗器械导致的伤害或死亡事件。
已上市的医疗器械,在非正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。
8.2.1 超产品注册证批准适用范围使用医疗器械
案例分享:
有源医疗器械案例:
例1:医院使用骨科X射线C型臂替代DSA对患者进行心脏/神经手术,从而导致在患者手术过程中,图像质量无法达标,导致手术时间延长,病人受到伤害。
无源医疗器械案例:
例1:输卵管导管插入术器械获批的适用范围为用于输卵管近端的选择性导管插入及输卵管造影,且说明书的注意事项明确描述输卵管导管插入术器械预期不用于输卵管完整导管插入术或输卵管再通术。但是该器械实际被用于进行输卵管近端介入再通术,临床复查中时发现输卵管导管插入术器械头端断裂残留在患者体内需要再次手术取出。
体外诊断医疗器械案例:
例1:总蛋白试剂盒说明书预期用途写明用于体外定量测定人血清和血浆的项目检测。但用户将该试剂盒用于尿液蛋白的检测,产生了不正确的检测结果。
8.2.2 超出使用寿命或有效期使用医疗器械
案例分享:
有源医疗器械案例:
例1:超出麻醉机的说明书所规定的其流量传感器的使用寿命使用麻醉机,导致手术过程中麻醉机故障,需要更换麻醉机,导致手术中断,病人手术时间延长。
无源医疗器械案例:
例1:使用过期的敷料导致患者感染。
体外诊断医疗器械案例:
例1:用户在生化仪电解质模块上使用了过期的电极,导致患者的电解质检测结果不正确。
8.2.3 其它
违规重复使用一次性无菌医疗器械、违规采购使用二手医疗器械设备等,导致患者伤害、死亡。
8.3 不可能导致死亡或伤害的事件
未导致死亡或伤害,并且如果事件再次发生,也不可能导致死亡或伤害的事件。
以下情况实际不可能导致死亡或者伤害的,不需要按照医疗器械不良事件报告:
(1) 在医疗设备预防性维护阶段、一次性使用医用耗材采购验收阶段和诊断试剂质控检测阶段等非临床使用前发现医疗器械缺陷
(2) 医疗器械保护措施正常发挥作用,从而提醒操作者及时处理异常状态,避免伤害
对于未涉及患者伤害的,符合质量投诉定义的事件,要通过质量投诉途径告知注册人。
注册人需要对收到的事件信息启动调查、分析及评估,调查评估结果表明该事件属于需要报告不良事件的,及时通过国家医疗器械不良事件监测信息系统报告。
案例分享:
有源医疗器械案例:
例1:在医疗设备预防性维护阶段,麻醉机开机自检未通过,被隔离并停止使用,未对患者造成伤害。类似问题总是可以通过使用前开机检查被发现,并被隔离,停止使用,不可能造成伤害。
无源医疗器械案例:
例1:医院采购部门在采购验收无菌纱布时,发现产品无菌包装破损或其它质量问题,拒收退换产品,类似产品质量问题总是可以通过常规检查被发现,产品可避免使用,不可能造成伤害。
体外诊断医疗器械案例:
例1:在医院检验科例行质控检测时,诊断试剂未通过质控检测,无法用于检测,未被临床使用,且类似产品质量问题总是可以通过质控检测被发现,产品可避免使用,可避免错误检测结果出现。
例2:检验科新启用某批次试剂时,按照说明书要求进行定标,仪器报警提示定标失败,该批次试剂不能用于临床检测,可避免错误检测结果出现。
8.4 非医疗器械原因导致的死亡或伤害
患者自身疾病导致的死亡或伤害。
案例分享:
无源医疗器械案例:
例1:患者为83岁男性,于左前降支近段和右冠远端各植入一枚冠脉支架,术后平稳于5天后出院。5年后,术者获知患者因为车祸死亡。
9. 医疗器械不良事件报告填写规范
医疗器械不良事件报告内容应真实、完整、准确。应真实记录所发现或获知的不良事件,不篡改、不主观臆断,严禁虚假报告。尽量获取不良事件的详细信息,如无法获得的信息不要编撰、不要推测。
使用单位、生产经营企业和个人在报告不良事件时,应当填写报告人并在系统中维护联系人和联系电话。
下表斜体字体为填写要求说明。
生产经营企业或使用单位医疗器械不良事件报告表(*为必填项)
报告基本情况
报告编码
系统自动生成
报告地
系统自动生成
1A报告人*
报告表的填写人或报告的发起人
1.医疗器械情况
a 产品名称*
输入产品注册证/备案凭证编号信息后会自动显示。
b 注册证编号*:
如果注册证信息没有录入系统,将无法上报!如遇该情况,请联系注册人或所在区市场局系统管理员。
国食药监械(准/进)字xxxx第xxxxxxx号、国械注准/进xxxxxxxxxxx、国械注许xxxxxxxxxxx
c 型号:
d 规格:
f 产品批号:
无源产品和诊断试剂请提供批号。
g 产品编号:
有源产品请提供编号或者序列号。
h UDI:
i生产日期:
j 有效期至:
大型设备可以忽略此项,但耗材和诊断试剂请务必填写。
上市许可持有人名称
输入产品注册证/备案凭证编号信息后会自动显示。
2.不良事件情况
k 事件发生日期*
如未知发生日期,可填写获知日期,并在s 使用过程中注明。
l 发现或获知日期*
m 伤害*
□死亡 □严重伤害 □其他(如可能导致死亡或严重伤害的医疗器械不良事件和/或故障)
伤害表现:非必填项,部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述伤害表现。
n 器械故障表现:部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述器械故障,注意与伤害表现有所区分。
o姓 名:
出生日期(选择)
选择日期
年龄类型:
岁、月、天
年龄
填写数字
既往病史
3.使用情况
p预期治疗疾病或作用:
是指涉及的医疗器械用于治疗的疾病或作用。
q 器械使用日期*:
r 使用场所*:
□医疗机构 □家庭 □其他
场所名称:
s 使用过程*:
对医疗器械实际使用过程的描述,按产品类别和实际情况尽可能提供,不超过 2000字。以下套用格式可以在填写时参考:
何时在何场所因何种原因开始使用何种医疗器械,使用情况如何,于何时出现何不良事件,给患者造成何种影响。何时采取何措施,何时不良事件表现治愈或好转。
t合并用药/械情况:
与所报告器械配合使用的某品牌、规格、型号的其他器械或药品。
4.事件初步原因分析与处置仅限经营企业或使用单位填写
u事件原因分析*:
□产品原因(包括说明书等)□操作原因□患者自身原因□无法确定
事件原因分析描述:
从产品质量、设计、运输保存、临床使用、患者疾病进展、合并用药械等方面分析。
初步处置情况*:
对患者和/或对器械的处置情况。
产品标签样张标识,仅供填写时参考:
无源产品:
有源产品:
IVD产品:
注册人医疗器械不良事件报告表
(*为必填项)
报告基本情况
报告编码:
系统自动生成
发生地:
境内
1.医疗器械情况
a 产品名称*
输入产品注册证/备案凭证编号信息后会自动显示。
b 注册证编号*:
如果注册证信息没有录入系统,将无法上报!如遇该情况,请联系所在区市场局系统管理员。
曾用注册证编号
自动填充
曾用注册证编号上报*:
□是 □否
c 型号:
XXXX
d 规格:
e产地*:
□进口 □国产 □港澳台 自动填充
产品类别*:
□有源 □无源 □体外诊断试剂 自动填充
管理类别*:
□III类 □II类 □I类 自动填充
f 产品批号:
无源产品和诊断试剂请提供批号。
g 产品编号:
有源产品请提供编号或者序列号。
h UDI:
i生产日期:
j 有效期至:
大型设备可以忽略此项,但耗材和诊断试剂请务必填写。
注册人(上市许可持有人)名称
输入产品注册证/备案凭证编号信息后会自动显示。
2.不良事件情况
k 事件发生日期*
如未知发生日期,可填写获知日期,并在s 使用过程中注明。
l 发现或获知日期*
m 伤害*
□死亡 □严重伤害 □其他(如濒临事件和/或故障)
伤害表现:非必填项,部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用简洁语言描述伤害表现。
n 器械故障表现:部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述器械故障,注意与伤害表现有所区分。
o姓 名:
出生日期(选择)
年龄类型:
年龄
性 别:□男 □女
病历号:
既往病史:
3.使用情况
p预期治疗疾病或作用:
是指涉及的医疗器械用于治疗的疾病或作用。
q 器械使用日期*:
r 使用场所*:
□医疗机构 □家庭 □其他
场所名称:
s 使用过程*:
对医疗器械实际使用过程的描述,按产品类别和实际情况尽可能提供,不超过2000字。以下套用格式可以在填写时参考:
何时在何场所因何种原因开始使用何种医疗器械,使用情况如何,于何时出现何不良事件,给患者造成何种影响。何时采取何措施,何时不良事件表现治愈或好转。
t合并用药/械情况:
与所报告器械配合使用的某品牌、规格、型号的其他器械或药品。
4.事件调查
v是否展开了调查*:
□是 □否
调查情况:
(可上传附件):调查情况可包含生产记录调查结果,医院使用情况,对退回的样品进行分析,抱怨趋势分析,设备维护保养状态等。
是否填写报告评价*:
□是 □否
5.评价结果
w关联性评价*:
□与产品有关□与产品无关□无法确定
x事件原因分析*:
(可上传附件):需阐述是否涉及产品使用安全。
y是否需要开展产品风险评价*
□是□否 选择是请填写“计划提交时间”
出现以下情况之一,注册人应进行产品风险评价:
– 已知的不良事件,其发生概率超出预期;
– 出现新的、未知不良事件;
– 监管部门提示产品可能存在风险的;
– 其它。
计划提交时间:
6.控制措施
z是否采取了控制措施*:
□是□否
具体控制措施描述:
(可上传附件):为控制或降低系统性风险而对器械和/或配合使用单位采取的措施。
未采取控制措施原因:
7.错报误报
是否错报误报*:
□是 □否 若选择“是”,请填写错报误报原因
错报误报原因*
8.报告合并
是否合并报告*
□是 □否 若选择“是”,请填写合并报告编码
合并报告编码*
9.1医疗器械情况
a. 产品名称*:填写时应与医疗器械注册证/备案凭证中产品名称保持一致,可根据产品说明书、标签等进行填写
b. 注册证编号*:指不良事件涉及医疗器械注册证中的注册证/备案凭证编号,可根据产品说明书、标签等进行填写
c. 型号:医疗器械注册证中列明型号
d. 规格:医疗器械注册证中列明的规格,需根据医疗器械产品标签等如实填写
e. 产地,产品类别和管理类别等信息为注册人维护,输入产品信息后会自动显示
f. 产品批号:如按批号管理的医疗器械产品必填,需根据产品标签等如实填写
g. 产品编号:如按序列号管理的医疗器械必填,需根据设备上的标识等如实填写
h. UDI:唯一器械标识,适用者填写
i. 生产日期:需根据医疗器械产品标签等如实填写
j. 有效期至:需根据医疗器械产品标签等如实填写
9.2不良事件情况
k. 事件发生日期*:事件实际发生日期,如仅知道事件发生年份,可填写当年的1月1日,如仅知道年份和月份,可填写当月的第1日,如未知发生日期,可填写事件知晓日期,以上情况需在s项使用过程中注明
l. 发现或获知日期*:是指报告单位发现或知道医疗器械不良事件的确切时间
m. 伤害*:
严重伤害:参考术语解释
其他:是指濒临事件或创新医疗器械在首个注册期内发生的非死亡和严重伤害的其他有害事件
伤害表现:指不良事件发生后对患者造成的具体伤害表现,例如二次手术、额外出血等。如对患者无伤害应注明无伤害
n. 器械故障表现:故障参考“术语解释”。
o. 姓名、年龄、性别、病例号:当患者的下列至少一项信息可获得,即认为患者可识别。
年龄:是指患者发生可疑医疗器械不良事件时的实际年龄,字体为阿拉伯数字。若患者年龄小于1岁,应填写具体的月份或天数,如6个月。
既往病史:既往病史指过去曾患过某种严重疾病如结核病、精神病等,或有较严重的先天性疾病如先天性心脏病等,或做过较大手术如先天性心脏病手术或肝、胆、胰、脾、肾等主要脏器手术,还可能包括患者住院史、过敏和吸烟史等。轻度医疗干预治疗的病症不算既往病史。如服用药物治疗感冒等。
9.3使用情况
p. 预期治疗疾病或作用:
是指涉及不良事件的医疗器械用于治疗的疾病或作用。可按照产品注册证的预期用途填写。
q. 器械使用日期*:
指与不良事件相关的医疗器械使用日期,如仅知道事件发生年份,可填写当年的1月1日,如仅知道年份和月份,可填写当月的第1日,如未知发生日期,可填写事件知晓日期,以上情况需在u项使用过程中注明
r. 使用场所*:
指涉及不良事件的医疗器械的实际使用场所,填写时请选择相应的选项。若选择的是其他,请注明具体使用场所
s. 使用过程*:对医疗器械实际使用过程的描述,按产品类别和实际情况尽可能提供:
无源、有源医疗器械:
– 医疗器械使用情况
– 出现了什么样的非预期结果
– 对患者造成什么程度的影响
– 采取了哪些相应治疗措施,结果如何
体外诊断医疗器械:
– 涉及试剂的批号和效期
– 所有的患者测试结果,包括测定的日期和时间,检测结果数值及单位
– 其他确认或比对方法所得结果(如有)
– 包括检测结果数值及单位、日期和时间、是否正常和正常值的参考范围
– 当报告检测结果差异时,请明确为何怀疑或确定该项结果有可能错误。
– 解释说明哪个结果被判定为正确,是否被报告临床
– 患者医疗背景信息-如:是否怀孕、确诊疾病、相关用药情况
t. 合并用药/械情况:
是涉及不良事件的产品需要配套使用的其他医疗器械(不包括不良事件涉及的医疗器械)或药物。体外诊断产品应提供相关试剂、设备及耗材,并列明相关批号或序列号。
9.4事件初步原因分析与处置(仅限生产经营企业和使用单位报告)
u. 事件原因分析*:
– 产品原因:指医疗器械的使用与不良事件的发生存在合理的时间关系,从产品的机理、使用过程等进行综合分析,初步确认事件与产品存在联系。该情况包含说明书未明确指明使用方法等
– 操作原因:指医疗器械不良事件的发生与使用单位错误操作相关,错误操作是指在说明书撰写合理充分的情况下未按照说明书使用
– 患者自身原因:医疗器械正常发挥了其预期功能,完全由于患者自身疾病导致的不良事件
– 无法确定:不良事件重要信息不齐全或无法获得,不能判断医疗器械不良事件发生原因
事件原因分析描述:
可从以下方面进行分析描述:产品质量、临床使用、患者疾病进展、并用药械等,如现有信息无法完成分析原因,可先行填写初步分析结论或说明,待信息更新后补充
初步处置情况*:
事件发生后所采取的相应处理措施及结果。例如,更换产品等
9.5事件调查(仅限注册人报告)
v. 是否展开了调查*:
调查情况(可上传附件):
有源、无源尽可能包括以下方面(如有):
– 生产记录调查结果
– 医院使用情况
– 对退回的样品进行分析
– 抱怨趋势分析
– 设备维护保养状态
体外诊断医疗器械尽可能包括以下方面:
– 定标记录和质控记录
– 样本前处理分析情况(如样本离心时间、转速等)
- 设备维护保养状态和日常警报记录
是否填写报告评价*:
注册人完成不良事件调查、分析和评价,可报告评价结果时,本选项选“是”,继续填写报告剩余部分。
9.6评价结果(仅限注册人报告)
w. 关联性评价*:
以下为名词解释,指导上方勾选:
– 与产品有关:指医疗器械的使用与不良事件的发生存在合理关系,从产品的机理、使用过程等进行综合分析,初步确认事件与产品存在联系。
– 与产品无关:指医疗器械的使用与不良事件的发生无关,有明确的其他原因造成事件发生,例如:使用者操作原因、患者自身原因等。
– 无法确定:不良事件重要信息不齐全或无法获得,不能判断医疗器械不良事件发生原因。
x. 事件原因分析*(可上传附件):
注册人应广泛收集不良事件信息,如现有信息无法完成原因分析,注册人可先行填写初步分析结论或说明,待完成相关调查跟踪及资料汇总后,提交最终结论。
根据调查获得的信息进行分析描述,可从产品原因、操作原因、患者自身原因和其他可能原因分析。如因不良事件重要信息不齐全或无法获得,原因无法确定,请说明情况。
y. 是否需要开展产品风险评价:
注册人应进行原因分析和关联性评价,若医疗器械存在风险的,注册人应开展产品风险评价。国家医疗器械不良事件监测信息系统预警,提示产品可能存在风险的,注册人也应开展相关产品的风险评价。
9.7控制措施(仅限注册人报告)
z. 是否采取了控制措施*:
具体控制措施描述(可上传附件):
事件发生后,针对事件原因所采取的相应措施,从而减少再次发生的风险。
所采取的相应处理措施及结果。例如,更换产品、培训用户等
未采取控制措施原因:
如未采取控制措施须写明为何不用采取措施的原因。
10. 参考文件
[1] 《医疗器械监督管理条例》(中华人民共和国国务院令 第739号)
[2] 《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局 中华人民共和国国家卫生健康委员会令 第1号)
[3] 《药物临床试验期间安全性数据快速报告标准和程序》(中华人民共和国 药品评审中心)
[4] GHTF/SG2/N54R8:Medical Devices Post Market Surveillance: Global Guidance for Adverse Event Reporting for Medical Devices, November 30,2006
[5] Medical Device Reporting for Manufacturers:Guidance for Industry and Food and Drug Administration Staff, November 8, 2016
[6] GB/T 42061-2022《医疗器械 质量管理体系用于法规的要求》
[7] GB/T 42062-2022 《医疗器械 风险管理对医疗器械的应用》
[8] Medical Device Reporting(MDR)21 CFR Part 803 (http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=803)
[9] The Guidance Document for Mandatory Problem Reporting for Medical Devices.(http://www.hc-sc.gc.ca/dhp-mps/pubs/medeff/_guide/2011-devices-materiaux/index-eng.php)
[10] 广东省药品监督管理局关于发布《医疗器械不良事件监测和再评价管理办法》及监测信息系统操作常见问题答疑
[11] 上海市药品和医疗器械不良反应监测中心器械监测微信公众号“上海药物警戒”
11. 附录
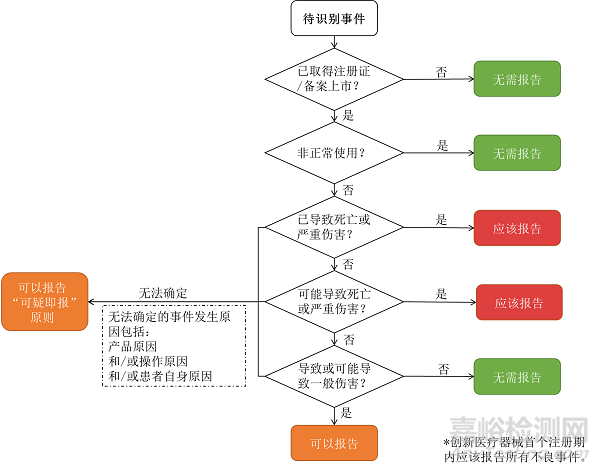
11.1 附录一:个例医疗器械不良事件报告决策树
严重伤害:是指有下列情况之一者:
(1) 危及生命:在此是指在发生不良事件时患者已经处于死亡的危险中,并不是指假设该不良事件如果更严重可能导致死亡。
(2) 导致机体功能的永久性伤害或者机体结构的永久性损伤。
(3) 必须采取医疗措施干预才能避免上述永久性伤害或者损伤。
一般伤害:不属于医疗器械死亡及严重伤害范围内的其他导致或者可能导致人体伤害的各种有害事件。
11.2 附录二:不良事件报告填写案例
生产经营企业或使用单位医疗器械不良事件报告表填写案例
报告基本情况
报告编码:
XXXXXXXXXXX
报告日期:
20XX年XX月XX日
报告人*:
XXX
单位名称:
XXXX医院
联系地址:
XXXXXXXXXXXX
联系人:
XXX
联系电话:
XXXXXXXX
发生地:
境内
1.医疗器械情况
a 产品名称*
XXXXXXXXXX
b 注册证编号*:
国械注进XXXXXXXXXXX
c 型号:
XXXX
d 规格:
e产地*:
■进口 □国产 □港澳台
产品类别*:
■有源 □无源 □体外诊断试剂
管理类别*:
■III类 □II类 □I类
f 产品批号:
g 产品编号:
XXXXX
h UDI:
i生产日期:
20XX-XX-XX
j 有效期至:
20XX-XX-XX
注册人(上市许可持有人)名称
XXXXXXXXXX公司
2.不良事件情况
k 事件发生日期*
20XX-XX-XX
l 发现或获知日期*
20XX-XX-XX
m 伤害*
□死亡 □严重伤害 █其他
伤害表现:无
n 器械故障表现:治疗床自动升起。
o姓 名:
XXX
出生日期(选择)
年龄类型:
年龄
XX
性 别:█男 □女
病历号:
既往病史
3.使用情况
p预期治疗疾病或作用:
医用直线加速器临床用于肿瘤的放射治疗。
q 器械使用日期*:
20XX-XX-XX
r 使用场所*:
█医疗机构 □家庭 □其他
场所名称:
XXXX医院
s 使用过程*:
XX医院于20XX年安装该设备,20XX年X月X日,当患者正接受治疗时,病床 自动升起并不断上升至患者碰到了设备上部的附件框,医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。
t合并用药/械情况:
无
4.事件初步原因分析与处置 仅限经营企业或使用单位填写
u事件原因分析*:
█产品原因(包括说明书等)□操作原因 □患者自身原因□无法确定
事件原因分析描述:
现场维修工程师初步判定:床的基座由于雨水倒灌,造成短路,床因此自 动升起。
初步处置情况*:
医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁 阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未 发现患者因病床上升受到身体伤害。
注册人(上市许可持有人)医疗器械不良事件报告表填写案例
报告基本情况
报告编码:
XXXXXXXXXXX
报告日期:
20XX年XX月XX日
报告人*:
XXX
单位名称:
XXXX医院
联系地址:
XXXXXXXXXXXX
联系人:
XXX
联系电话:
XXXXXXXX
发生地:
境内
1.医疗器械情况
a 产品名称*
XXXXXXXXXX
b 注册证编号*:
国械注进XXXXXXXXXXX
c 型号:
XXXX
d 规格:
e产地*:
■进口 □国产 □港澳台
产品类别*:
■有源 □无源 □体外诊断试剂
管理类别*:
■III类 □II类 □I类
f 产品批号:
g 产品编号:
XXXXX
h UDI:
i生产日期:
20XX-XX-XX
j 有效期至:
20XX-XX-XX
注册人(上市许可持有人)名称
XXXXXXXXXX公司
2.不良事件情况
k 事件发生日期*
20XX-XX-XX
l 发现或获知日期*
20XX-XX-XX
m 伤害*
□死亡 □严重伤害 █其他
伤害表现:无
n 器械故障表现:治疗床自动升起。
o姓 名:
XXX
出生日期(选择)
年龄类型:
年龄
XX
性 别:█男 □女
病历号:
既往病史
3.使用情况
p预期治疗疾病或作用:
医用直线加速器临床用于肿瘤的放射治疗。
q 器械使用日期*:
20XX-XX-XX
r 使用场所*:
█医疗机构 □家庭 □其他
场所名称:
XXXX医院
s 使用过程*:
XX医院于20XX年安装该设备,20XX年X月X日,当患者正接受治疗时,病床 自动升起并不断上升至患者碰到了设备上部的附件框,医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。
t合并用药/械情况:
无
4.事件调查
v是否展开了调查*:
█是 □否
调查情况:
(可上传附件):
经XX公司专家团队调查后发现:
XX医院于20XX年安装和调试该设备,XX公司末次现场维修时间为20XX年XX月XX日。
本次事件发生后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。
XX公司已组织技术组对该事件进行调查分析,结论为该事件系床的基座浸入雨水造成短路所致。
截止到目前为止,在中国境内的同类产品未曾发生过类似事件。
XX公司将发布一封客户告知信(内部编号为:XXXX-XX-XX),以告知中国客户将对该台设备安装浮止装置,如果安装了浮止装置,即使雨水浸入基座,浮止装置一旦漂浮起来,则设备会自动断电。
XX公司将准备一项现场纠正措施(内部编号为:XXXX-XX-XX)对该台设备安装浮止装置以解决此潜在问题。
XX公司将近期为该台设备补装浮止装置。
是否填写报告评价*:
█是 □否
5.评价结果
w关联性评价*:
█与产品有关□与产品无关□无法确定
x事件原因分析*:
(可上传附件):需阐述是否涉及产品使用安全。
y是否需要开展产品风险评价*
█是□否
以下风险评价报告只是演示样例,实际应在系统的“产品风险评价报告”模块中提交:
XX公司已组织技术组对该事件进行调查分析,结论为该事件系床的基座浸入雨水造成短路所致。
风险评价简述:
1. 由于基建要求系统安装必须处于室内,并由医院施工团队验收,遭受雨水渗透可能性较低。
2. 截止到目前为止,在中国境内的同类的未曾发生过类似事件。
3. 根据全球装机量及使用情况,结合同样原因导致的雨水浸入设备情况数据可得出:该事件发生的概率较低。
4. 操作者并不被鼓励在室内环境有雨水的情况下使用仪器,以防触电危害的发生。
基于以上的风险分析,风险评估结果为XX(风险严重程度为X,发生概率为X)。
计划提交时间:
20XX-XX-XX
6.控制措施
z是否采取了控制措施*:
█是□否
具体控制措施描述:
(可上传附件):为控制或降低系统性风险而对器械和/或配合使用单位采取的措施。
未采取控制措施原因:
7.错报误报
是否错报误报*:
□是█否
8.报告合并
是否合并报告*
□是█否
11.3 附录三:监测信息系统常见问题答疑
见微信公众号“上海药物警戒”
刚刚,上海市药品监督管理局发布《上海市个例医疗器械不良事件报告指南(2023年修订版)》,内容如下:
|
报告基本情况 |
||||||
|
报告编码 |
系统自动生成 |
|||||
|
报告地 |
系统自动生成 |
|||||
|
1A报告人* |
报告表的填写人或报告的发起人 |
|||||
|
1.医疗器械情况 |
||||||
|
a 产品名称* |
输入产品注册证/备案凭证编号信息后会自动显示。 |
|||||
|
b 注册证编号*: |
如果注册证信息没有录入系统,将无法上报!如遇该情况,请联系注册人或所在区市场局系统管理员。 国食药监械(准/进)字xxxx第xxxxxxx号、国械注准/进xxxxxxxxxxx、国械注许xxxxxxxxxxx |
|||||
|
c 型号: |
|
|||||
|
d 规格: |
|
|||||
|
f 产品批号: |
无源产品和诊断试剂请提供批号。 |
|||||
|
g 产品编号: |
有源产品请提供编号或者序列号。 |
|||||
|
h UDI: |
|
|||||
|
i生产日期: |
|
|||||
|
j 有效期至: |
大型设备可以忽略此项,但耗材和诊断试剂请务必填写。 |
|||||
|
上市许可持有人名称 |
输入产品注册证/备案凭证编号信息后会自动显示。 |
|||||
|
2.不良事件情况 |
||||||
|
k 事件发生日期* |
如未知发生日期,可填写获知日期,并在s 使用过程中注明。 |
|||||
|
l 发现或获知日期* |
|
|||||
|
m 伤害* |
□死亡 □严重伤害 □其他(如可能导致死亡或严重伤害的医疗器械不良事件和/或故障) |
|||||
|
伤害表现:非必填项,部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述伤害表现。
|
||||||
|
n 器械故障表现:部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述器械故障,注意与伤害表现有所区分。
|
||||||
|
o姓 名: |
|
出生日期(选择) |
选择日期 |
|||
|
年龄类型: |
岁、月、天 |
年龄 |
填写数字 |
|||
|
既往病史 |
|
|||||
|
3.使用情况 |
||||||
|
p预期治疗疾病或作用: |
是指涉及的医疗器械用于治疗的疾病或作用。 |
|||||
|
q 器械使用日期*: |
|
|||||
|
r 使用场所*: |
□医疗机构 □家庭 □其他 |
场所名称: |
|
|||
|
s 使用过程*: |
对医疗器械实际使用过程的描述,按产品类别和实际情况尽可能提供,不超过 2000字。以下套用格式可以在填写时参考: 何时在何场所因何种原因开始使用何种医疗器械,使用情况如何,于何时出现何不良事件,给患者造成何种影响。何时采取何措施,何时不良事件表现治愈或好转。 |
|||||
|
t合并用药/械情况: |
与所报告器械配合使用的某品牌、规格、型号的其他器械或药品。 |
|||||
|
4.事件初步原因分析与处置仅限经营企业或使用单位填写 |
||||||
|
u事件原因分析*: |
□产品原因(包括说明书等)□操作原因□患者自身原因□无法确定 |
|||||
|
事件原因分析描述:
|
从产品质量、设计、运输保存、临床使用、患者疾病进展、合并用药械等方面分析。 |
|||||
|
初步处置情况*: |
对患者和/或对器械的处置情况。 |
|||||



|
报告基本情况 |
||||||
|
报告编码: |
系统自动生成 |
|||||
|
发生地: |
境内 |
|||||
|
1.医疗器械情况 |
||||||
|
a 产品名称* |
输入产品注册证/备案凭证编号信息后会自动显示。 |
|||||
|
b 注册证编号*: |
如果注册证信息没有录入系统,将无法上报!如遇该情况,请联系所在区市场局系统管理员。 |
|||||
|
曾用注册证编号 |
自动填充 |
|||||
|
曾用注册证编号上报*: |
□是 □否 |
|||||
|
c 型号: |
XXXX |
|||||
|
d 规格: |
|
|||||
|
e产地*: |
□进口 □国产 □港澳台 自动填充 |
|||||
|
产品类别*: |
□有源 □无源 □体外诊断试剂 自动填充 |
|||||
|
管理类别*: |
□III类 □II类 □I类 自动填充 |
|||||
|
f 产品批号: |
无源产品和诊断试剂请提供批号。 |
|||||
|
g 产品编号: |
有源产品请提供编号或者序列号。 |
|||||
|
h UDI: |
|
|||||
|
i生产日期: |
|
|||||
|
j 有效期至: |
大型设备可以忽略此项,但耗材和诊断试剂请务必填写。 |
|||||
|
注册人(上市许可持有人)名称 |
输入产品注册证/备案凭证编号信息后会自动显示。 |
|||||
|
2.不良事件情况 |
||||||
|
k 事件发生日期* |
如未知发生日期,可填写获知日期,并在s 使用过程中注明。 |
|||||
|
l 发现或获知日期* |
|
|||||
|
m 伤害* |
□死亡 □严重伤害 □其他(如濒临事件和/或故障) |
|||||
|
伤害表现:非必填项,部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用简洁语言描述伤害表现。
|
||||||
|
n 器械故障表现:部分产品数据库已开放,请尽可能在系统中选择。如无法选择,请用极简洁语言描述器械故障,注意与伤害表现有所区分。
|
||||||
|
o姓 名: |
|
出生日期(选择) |
|
|||
|
年龄类型: |
|
年龄 |
|
|||
|
性 别:□男 □女 |
病历号: |
|||||
|
既往病史: |
|
|||||
|
3.使用情况 |
||||||
|
p预期治疗疾病或作用: |
是指涉及的医疗器械用于治疗的疾病或作用。 |
|||||
|
q 器械使用日期*: |
|
|||||
|
r 使用场所*: |
□医疗机构 □家庭 □其他 |
场所名称: |
|
|||
|
s 使用过程*: |
对医疗器械实际使用过程的描述,按产品类别和实际情况尽可能提供,不超过2000字。以下套用格式可以在填写时参考: 何时在何场所因何种原因开始使用何种医疗器械,使用情况如何,于何时出现何不良事件,给患者造成何种影响。何时采取何措施,何时不良事件表现治愈或好转。 |
|||||
|
t合并用药/械情况: |
与所报告器械配合使用的某品牌、规格、型号的其他器械或药品。 |
|||||
|
4.事件调查 |
||||||
|
v是否展开了调查*: |
□是 □否 |
|||||
|
调查情况:
|
(可上传附件):调查情况可包含生产记录调查结果,医院使用情况,对退回的样品进行分析,抱怨趋势分析,设备维护保养状态等。 |
|||||
|
是否填写报告评价*: |
□是 □否 |
|||||
|
5.评价结果 |
||||||
|
w关联性评价*: |
□与产品有关□与产品无关□无法确定 |
|||||
|
x事件原因分析*: |
(可上传附件):需阐述是否涉及产品使用安全。 |
|||||
|
y是否需要开展产品风险评价* |
□是□否 选择是请填写“计划提交时间” 出现以下情况之一,注册人应进行产品风险评价: – 已知的不良事件,其发生概率超出预期; – 出现新的、未知不良事件; – 监管部门提示产品可能存在风险的; – 其它。 |
|||||
|
计划提交时间: |
|
|||||
|
6.控制措施 |
||||||
|
z是否采取了控制措施*: |
□是□否 |
|||||
|
具体控制措施描述: |
(可上传附件):为控制或降低系统性风险而对器械和/或配合使用单位采取的措施。 |
|||||
|
未采取控制措施原因: |
|
|||||
|
7.错报误报 |
||||||
|
是否错报误报*: |
□是 □否 若选择“是”,请填写错报误报原因 |
|||||
|
错报误报原因* |
|
|||||
|
8.报告合并 |
||||||
|
是否合并报告* |
□是 □否 若选择“是”,请填写合并报告编码 |
|||||
|
合并报告编码* |
|
|||||
|
报告基本情况 |
||||||
|
报告编码: |
XXXXXXXXXXX |
|||||
|
报告日期: |
20XX年XX月XX日 |
|||||
|
报告人*: |
XXX |
|||||
|
单位名称: |
XXXX医院 |
|||||
|
联系地址: |
XXXXXXXXXXXX |
|||||
|
联系人: |
XXX |
|||||
|
联系电话: |
XXXXXXXX |
|||||
|
发生地: |
境内 |
|||||
|
1.医疗器械情况 |
||||||
|
a 产品名称* |
XXXXXXXXXX |
|||||
|
b 注册证编号*: |
国械注进XXXXXXXXXXX |
|||||
|
c 型号: |
XXXX |
|||||
|
d 规格: |
|
|||||
|
e产地*: |
■进口 □国产 □港澳台 |
|||||
|
产品类别*: |
■有源 □无源 □体外诊断试剂 |
|||||
|
管理类别*: |
■III类 □II类 □I类 |
|||||
|
f 产品批号: |
|
|||||
|
g 产品编号: |
XXXXX |
|||||
|
h UDI: |
|
|||||
|
i生产日期: |
20XX-XX-XX |
|||||
|
j 有效期至: |
20XX-XX-XX |
|||||
|
注册人(上市许可持有人)名称 |
XXXXXXXXXX公司 |
|||||
|
2.不良事件情况 |
||||||
|
k 事件发生日期* |
20XX-XX-XX |
|||||
|
l 发现或获知日期* |
20XX-XX-XX |
|||||
|
m 伤害* |
□死亡 □严重伤害 █其他 |
|||||
|
伤害表现:无 |
||||||
|
n 器械故障表现:治疗床自动升起。 |
||||||
|
o姓 名: |
XXX |
出生日期(选择) |
|
|||
|
年龄类型: |
|
年龄 |
XX |
|||
|
性 别:█男 □女 |
病历号: |
|||||
|
既往病史 |
|
|||||
|
3.使用情况 |
||||||
|
p预期治疗疾病或作用: |
医用直线加速器临床用于肿瘤的放射治疗。 |
|||||
|
q 器械使用日期*: |
20XX-XX-XX |
|||||
|
r 使用场所*: |
█医疗机构 □家庭 □其他 |
场所名称: |
XXXX医院 |
|||
|
s 使用过程*: |
XX医院于20XX年安装该设备,20XX年X月X日,当患者正接受治疗时,病床 自动升起并不断上升至患者碰到了设备上部的附件框,医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。 |
|||||
|
t合并用药/械情况: |
无 |
|||||
|
4.事件初步原因分析与处置 仅限经营企业或使用单位填写 |
||||||
|
u事件原因分析*: |
█产品原因(包括说明书等)□操作原因 □患者自身原因□无法确定 |
|||||
|
事件原因分析描述:
|
现场维修工程师初步判定:床的基座由于雨水倒灌,造成短路,床因此自 动升起。 |
|||||
|
初步处置情况*: |
医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁 阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未 发现患者因病床上升受到身体伤害。 |
|||||
注册人(上市许可持有人)医疗器械不良事件报告表填写案例
|
报告基本情况 |
||||||
|
报告编码: |
XXXXXXXXXXX |
|||||
|
报告日期: |
20XX年XX月XX日 |
|||||
|
报告人*: |
XXX |
|||||
|
单位名称: |
XXXX医院 |
|||||
|
联系地址: |
XXXXXXXXXXXX |
|||||
|
联系人: |
XXX |
|||||
|
联系电话: |
XXXXXXXX |
|||||
|
发生地: |
境内 |
|||||
|
1.医疗器械情况 |
||||||
|
a 产品名称* |
XXXXXXXXXX |
|||||
|
b 注册证编号*: |
国械注进XXXXXXXXXXX |
|||||
|
c 型号: |
XXXX |
|||||
|
d 规格: |
|
|||||
|
e产地*: |
■进口 □国产 □港澳台 |
|||||
|
产品类别*: |
■有源 □无源 □体外诊断试剂 |
|||||
|
管理类别*: |
■III类 □II类 □I类 |
|||||
|
f 产品批号: |
|
|||||
|
g 产品编号: |
XXXXX |
|||||
|
h UDI: |
|
|||||
|
i生产日期: |
20XX-XX-XX |
|||||
|
j 有效期至: |
20XX-XX-XX |
|||||
|
注册人(上市许可持有人)名称 |
XXXXXXXXXX公司 |
|||||
|
2.不良事件情况 |
||||||
|
k 事件发生日期* |
20XX-XX-XX |
|||||
|
l 发现或获知日期* |
20XX-XX-XX |
|||||
|
m 伤害* |
□死亡 □严重伤害 █其他 |
|||||
|
伤害表现:无 |
||||||
|
n 器械故障表现:治疗床自动升起。 |
||||||
|
o姓 名: |
XXX |
出生日期(选择) |
|
|||
|
年龄类型: |
|
年龄 |
XX |
|||
|
性 别:█男 □女 |
病历号: |
|||||
|
既往病史 |
|
|||||
|
3.使用情况 |
||||||
|
p预期治疗疾病或作用: |
医用直线加速器临床用于肿瘤的放射治疗。 |
|||||
|
q 器械使用日期*: |
20XX-XX-XX |
|||||
|
r 使用场所*: |
█医疗机构 □家庭 □其他 |
场所名称: |
XXXX医院 |
|||
|
s 使用过程*: |
XX医院于20XX年安装该设备,20XX年X月X日,当患者正接受治疗时,病床 自动升起并不断上升至患者碰到了设备上部的附件框,医护人员发现后立刻使用紧急按钮停止设备运作,随后关机并拆卸了电磁阀油压阀门,病床被卸油后落下。随后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。 |
|||||
|
t合并用药/械情况: |
无 |
|||||
|
4.事件调查 |
||||||
|
v是否展开了调查*: |
█是 □否 |
|||||
|
调查情况:
|
(可上传附件): 经XX公司专家团队调查后发现: XX医院于20XX年安装和调试该设备,XX公司末次现场维修时间为20XX年XX月XX日。 本次事件发生后,医院对患者进行必要的检查,未发现患者因病床上升受到身体伤害。 XX公司已组织技术组对该事件进行调查分析,结论为该事件系床的基座浸入雨水造成短路所致。 截止到目前为止,在中国境内的同类产品未曾发生过类似事件。 XX公司将发布一封客户告知信(内部编号为:XXXX-XX-XX),以告知中国客户将对该台设备安装浮止装置,如果安装了浮止装置,即使雨水浸入基座,浮止装置一旦漂浮起来,则设备会自动断电。 XX公司将准备一项现场纠正措施(内部编号为:XXXX-XX-XX)对该台设备安装浮止装置以解决此潜在问题。 XX公司将近期为该台设备补装浮止装置。 |
|||||
|
是否填写报告评价*: |
█是 □否 |
|||||
|
5.评价结果 |
||||||
|
w关联性评价*: |
█与产品有关□与产品无关□无法确定 |
|||||
|
x事件原因分析*: |
(可上传附件):需阐述是否涉及产品使用安全。 |
|||||
|
y是否需要开展产品风险评价* |
█是□否 以下风险评价报告只是演示样例,实际应在系统的“产品风险评价报告”模块中提交: XX公司已组织技术组对该事件进行调查分析,结论为该事件系床的基座浸入雨水造成短路所致。 风险评价简述: 1. 由于基建要求系统安装必须处于室内,并由医院施工团队验收,遭受雨水渗透可能性较低。 2. 截止到目前为止,在中国境内的同类的未曾发生过类似事件。 3. 根据全球装机量及使用情况,结合同样原因导致的雨水浸入设备情况数据可得出:该事件发生的概率较低。 4. 操作者并不被鼓励在室内环境有雨水的情况下使用仪器,以防触电危害的发生。 基于以上的风险分析,风险评估结果为XX(风险严重程度为X,发生概率为X)。 |
|||||
|
计划提交时间: |
20XX-XX-XX |
|||||
|
6.控制措施 |
||||||
|
z是否采取了控制措施*: |
█是□否 |
|||||
|
具体控制措施描述: |
(可上传附件):为控制或降低系统性风险而对器械和/或配合使用单位采取的措施。 |
|||||
|
未采取控制措施原因: |
|
|||||
|
7.错报误报 |
||||||
|
是否错报误报*: |
□是█否 |
|||||
|
8.报告合并 |
||||||
|
是否合并报告* |
□是█否 |
|||||
本文由广州佳誉医疗器械有限公司/佛山浩扬医疗器械有限公司联合编辑